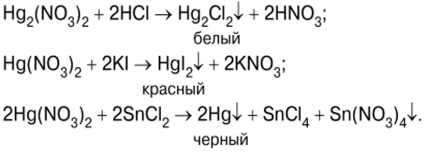
Реакції з'єднань ртуті
Металева ртуть та її сполуки високотоксичні для живих організмів. Особливо це стосується сполук, які добре розчиняються у воді. Слід виявляти велику обережність під час експериментування з комбінаціями цього унікального елемента (ртуть — єдиний метал, що у рідкому стані при кімнатній температурі). Дотримання основних заповідей хіміка? дозволить безпечно провести кілька експериментів із сполуками ртуті.
У першому досвіді отримуємо амальгаму алюмінію (розчин цього металу в рідкій ртуті). Розчин ртуті (II) Hg нітрату (V) Hg (NO3)2 та шматок алюмінієвого дроту (фото 1). Алюмінієвий стрижень (ретельно очищений від відкладень) поміщають у пробірку з розчином розчинної солі ртуті (фото 2). Через деякий час ми можемо спостерігати виділення бульбашок газу з поверхні дроту (фото 3 та 4). Після вилучення стрижня з розчину виявляється, що глина вкрита пухнастим нальотом, крім того, ми бачимо також кульки металевої ртуті (фото 5 і 6).
Хімія – досвід з'єднання ртуті
В нормальних умовах поверхня алюмінію вкрита щільно прилеглим шаром оксиду алюмінію.2O3ефективно ізолює метал від агресивного впливу довкілля. Після очищення та занурення стрижня в розчин ртутної солі іони Hg витісняються2+ більш активним алюмінієм:
Обложена на поверхні стрижня ртуть утворює амальгаму з алюмінієм, що ускладнює прилипання до нього оксиду. Алюміній - дуже активний метал (реагує з водою з виділенням водню - спостерігаються бульбашки газу), а його використання як конструкційний матеріал можливе завдяки щільному оксидному покриттю.
У другому експерименті ми виявимо іони NH амонію.4+ за допомогою реактиву Несслера (німецький хімік Юліус Несслер в 1856 першим застосував його в аналізі).
Експеримент з реакції хмелю та ртутних сполук
Випробування починається з осадження іодиду ртуті (II) HgI.2, після змішування розчинів іодиду калію KI та нітрату ртуті (II) (V) Hg (NO3)2 (фото 7):
Оранжево-червоний осад HgI2 (фото 8) потім обробляємо надлишком розчину йодиду калію до отримання розчинної комплексної сполуки формули К2HgI4 ? Тетраіодеркурат калію (II) (Фото 9), який є реактивом Несслера:
За допомогою отриманого з'єднання ми можемо виявити іони амонію. Як і раніше, потрібні розчини гідроксиду натрію NaOH і хлориду амонію NH.4Кл (фото 10). Після додавання до реактиву Несслера невеликої кількості розчину солі амонію та підлужування середовища сильною основою спостерігаємо утворення жовто-жовтогарячого забарвлення вмісту пробірки. Поточну реакцію можна записати рівнянням:
Отримане з'єднання ртуті має складну структуру:
Високочутливий тест Несслера використовується для виявлення навіть слідів солей амонію або аміаку у воді (наприклад, водопровідної воді).

